Licht kann als Welle aufgefasst werden, deren Schwingungsrichtung senkrecht zur Ausbreitungsrichtung steht. Schwingungs- und Ausbreitungsrichtung spannen eine Ebene auf, die Schwingungsebene.
Bei natürlichem Licht kommen alle möglichen Schwingungsebenen vor, d.h. es schwingt in allen Richtungen des Raumes senkrecht zur Ausbreitungsrichtung. Licht, das nur in einer Richtung schwingt, nennt man linear polarisiertes Licht. Es gibt nun lichtdurchlässige Substanzen, die aufgrund ihrer Struktur nur Licht in einer einzigen Schwingungsebene hindurchlassen. Sie wirken daher auf natürliches Licht wie ein Filter, der aus allen möglichen Schwingungsebenen eine bevorzugt und alle anderen ausfiltert. Solche „Filter“ nennt man Polarisationsfilter oder kurz Polarisator.
Geht polarisiertes Licht durch ein zweites Polarisationsfilter (genannt Analysator), so wird der Lichtstrahl dieses nur passieren können, falls Polarisator und Analysator die gleiche Schwingungsebene bevorzugen. Durch eine Drehung des Analysators senkrecht zur Ausbreitungsrichtung des Lichtes läßt sich dies erreichen. Schließen jedoch die Vorzugsebenen von Polarisator und Analysator einen Winkel von 90o ein, so wird der Lichtstrahl völlig ausgelöscht.
Stoffe, welche die Schwingungsebene von polarisiertem Licht drehen können, heißen optisch aktive Stoffe. Geräte zur Messung dieses Drehwinkels heißen Polarimeter.
Enantiomere drehen die Schwingungsebene des linear polarisierten Lichts um den gleichen Betrag (Winkel), aber in entgegengesetzter Richtung. Man spricht dabei von einer Rechtsdrehung, wenn die Polarisationsebene, gegen die Ausbreitungsrichtung des Lichtes gesehen, im Uhrzeigersinn gedreht wird. Eine Linksdrehung ist daher eine Drehung im Gegenuhrzeigersinn.
Rechtsdrehende Stoffe kennzeichnet man mit dem Zeichen (+) und linksdrehende mit dem Zeichen (-). [z.B. (+)-Milchsäure), D(-)-Milchsäure]. Die Drehrichtung eines Stoffes muß experimentell ermittelt werden und kann nicht aus der „D- oder L-From“ des Moleküls abgeleitet werden. D-Fructose dreht die Polarisationsebene nach links, D-Glucose nach rechts. Ein äquimolekulares Gemisch der links- und rechtsdrehenden Form eines Stoffes dreht die Polarisationsebene nicht, es ist optisch inaktiv und heißt Razemat [gekennzeichnet durch das Zeichen (±)].
Der Drehwinkel ![]() hängt ab von:
hängt ab von:
![]()
Der spezifische Drehwinkel errechnet sich somit wie folgt:
![]()
Für L(+)-Milchsäure gilt:
![]()
Für D(-)-Milchsäure gilt:
![]()
![]() -D-Glucose und
-D-Glucose und ![]() -D-Glucose unterscheiden sich nur durch die Stellung der
Hydroxylgruppe am anomeren C-Atom (ehemaliges Carbonyl-Kohlenstoffatom des
kettenförmigen Glucosemoleküls).
-D-Glucose unterscheiden sich nur durch die Stellung der
Hydroxylgruppe am anomeren C-Atom (ehemaliges Carbonyl-Kohlenstoffatom des
kettenförmigen Glucosemoleküls).
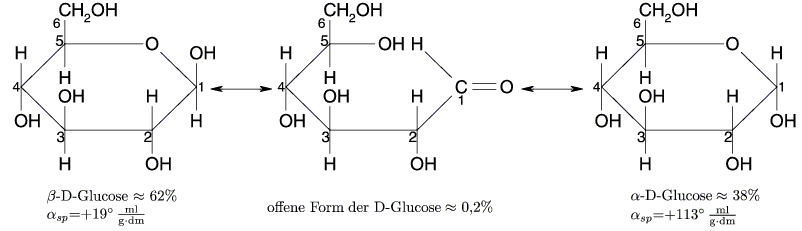
Löst man beide Anomeren getrennt in Wasser, so werden die angegebenen
Drehwinkel nur anfangs gemessen. Der Drehwinkel von ![]() -D-Glucose wird allmählich
immer größer, der von
-D-Glucose wird allmählich
immer größer, der von ![]() -D-Glucose immer kleiner, bis jeweils der spezifische
Enddrehwinkel von
-D-Glucose immer kleiner, bis jeweils der spezifische
Enddrehwinkel von ![]() = 54,7o erreicht ist. Diese Erscheinung der ständigen
Änderung des Drehwinkels bis zum Erreichen eines Enddrehwertes nennt man
Mutarotation. Ursache ist die Einstellung eines Gleichgewichts, bei dem sich
ringförmige
= 54,7o erreicht ist. Diese Erscheinung der ständigen
Änderung des Drehwinkels bis zum Erreichen eines Enddrehwertes nennt man
Mutarotation. Ursache ist die Einstellung eines Gleichgewichts, bei dem sich
ringförmige ![]() -D-Glucose über die Kettenform in die ringförmige
-D-Glucose über die Kettenform in die ringförmige ![]() -D-Glucose
umwandelt und umgekehrt. Im Gleichgewicht sind
-D-Glucose
umwandelt und umgekehrt. Im Gleichgewicht sind ![]() 62%
62% ![]() -D-Glucose,
-D-Glucose, ![]() 0,2% kettenförmige D-Glucose und
0,2% kettenförmige D-Glucose und ![]() 38%
38% ![]() -D-Glucose. Daraus ergibt sich:
-D-Glucose. Daraus ergibt sich:
![]()
(D-Glucose ![]() OH-Gruppe rechts)
OH-Gruppe rechts)
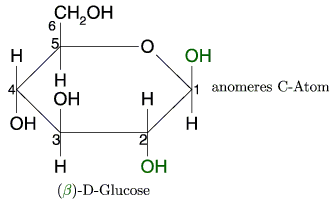
Anomere sind solche Isomere, die sich nur durch die Stellung der Hydroxylgruppe am
anomeren C-Atom unterscheiden. (C1 ![]() wo die neue OH-Gruppe gebildet
wurde!)
wo die neue OH-Gruppe gebildet
wurde!)
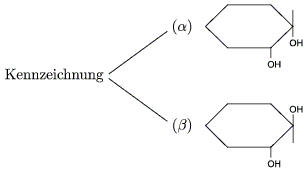
Wenn in der HAWORTH-Darstellung beide OH-Gruppen auf der gleichen Seite der
Sechseck-Ebene liegen, dann handelt es sich um ![]() -Glucose.
-Glucose. ![]() -Glucose ist es, wenn sie
auf verschiedenen Seiten liegen.
-Glucose ist es, wenn sie
auf verschiedenen Seiten liegen.
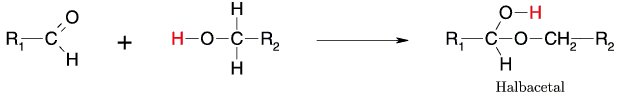
Er hat daher angenommen, daß die Aldehydgruppe der Glucose mit einer OH-Gruppe der Glucose reagiert und ein ringförmiges Halbacetal entsteht. Bei Glucose ist dies die OH-Gruppe am 5. C-Atom. Der Wasserstoff dieser OH-Gruppe wandert zum Sauerstoffatom der Aldehydgruppe. Am C-Atom 1 entsteht eine neue OH-Gruppe (Acetalhydroxyl).
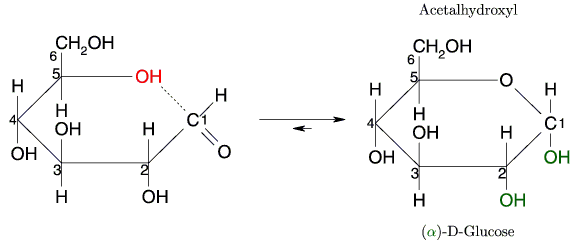
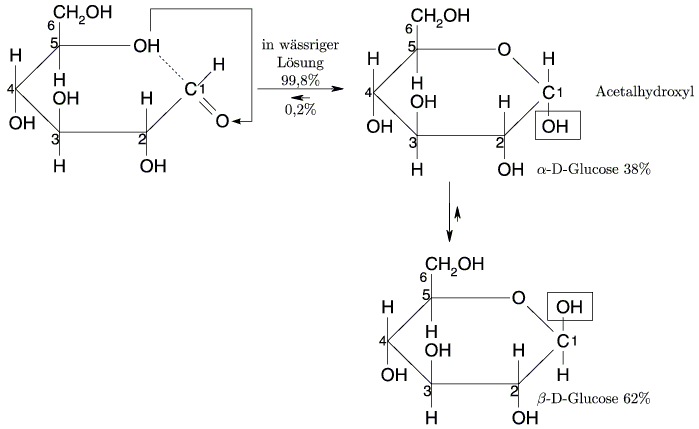
In wässriger (neutraler) Lösung steht die Kettenform und Ringform der Glucose in einem Gleichgewicht, das zu 99,8 % bei der Ringform liegt und zu 0,2 % bei der Kettenform.
