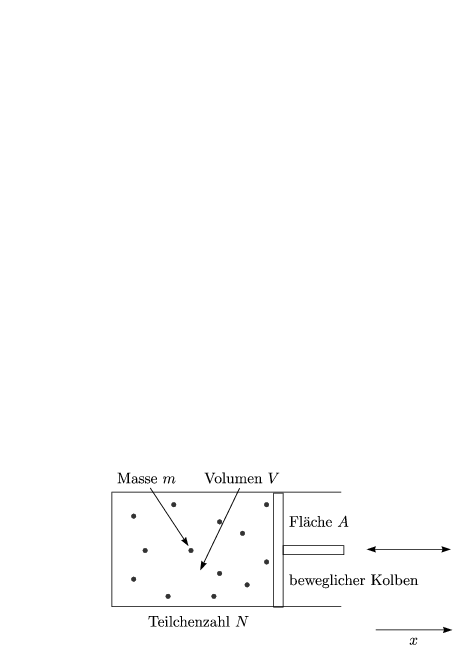
Ein ideales Gas ist eine große Anzahl von Teilchen (z.B. Atome oder Moleküle), deren gegenseitige Wechselwirkung klein aber nicht verschwindend ist. Normale Gase erfüllen diese Bedingung bei nicht zu niedrigen Temperaturen gut.

Verknüpfung der Zustandsgrößen p, V , T, N
Betrachten wir ein Zeitintervall dt:
Wie groß ist der Kraftstoß Fx dt? Haben die Teilchen zum Beispiel den Impuls pi,x,
gilt:
Es heißt hier 2pi,x aufgrund der Impulserhaltung, da das Teilchen die Richtung ändert. dN1 ist die Zahl der Teilchen, die im Zeitintervall dt mit dem Stempel stoßen, also dx vom Stempel entfernt sind (Dreisatz).
Der Faktor ![]() kommt daher, weil sich die Hälfte der Teilchen nach rechts und die
andere nach links bewegt.
kommt daher, weil sich die Hälfte der Teilchen nach rechts und die
andere nach links bewegt.
Es resultiert der folgende Druck:
Daraus folgt nun pi,x:
Summation über alle Impuls pi,x ergibt nun:

Beziehen wir die klassische Mechanik mit ein, so folgt für die kinetische Energie:
Aufgrund der Symmetrieeigenschaften ist keine Richtung von x, y und z ausgezeichnet. Daraus folgt das sogenannte Gleichverteilungsgesetz.
Oder auch mit der mittleren kinetischen Energie ![]() kin geschrieben:
kin geschrieben:
Daraus folgt:
Das Produkt p . V hängt somit nicht von der Verteilungsfunktion ab.