Bisher haben wir versucht, kbimolekular via der kinetischen Gastheorie herzuleiten. Jetzt wollen wir uns näher mit der Theorie des aktivierten Komplexes beschäftigen (läßt sich anwenden für kbimolekular und kunimolekular). Das Problem hier ist jedoch, daß uns wichtiges Detailwissen fehlt.
| Gibt es eine schlaue Näherung um mikroskopische Freiheitsgrade mitzunehmen ohne sämtliches Detailwissen? |
| Für k(T), Theorie des aktivierten Stoßkomplexes (via statistische Thermodynamik) |
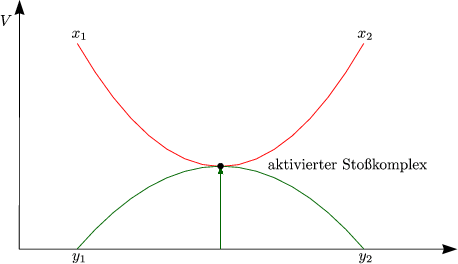
| Was ist ein aktivierter Stoßkomplex? Die Antwort erlangen wir über die Betrachtung von Potential(hyper)flächen. |
Wir nehmen an, daß nur kolineare Stöße zum Produkt führen.

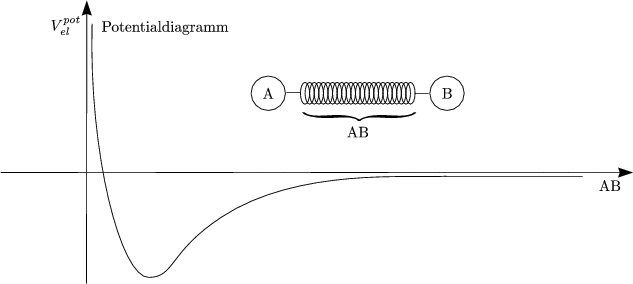
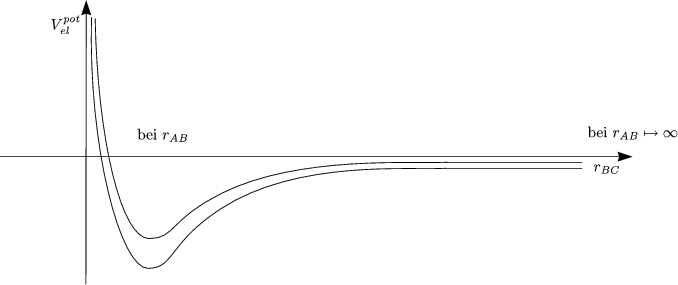
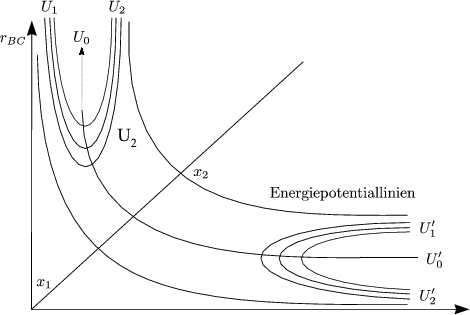
Klassisch findet bei der Schwingung eine Umwandlung von potentieller in kinetischer Energie statt. Für eine chemische Reaktion ist Uelpot bei festgehaltenem rBC und variablem rAB relevant. M.LONDON, H.EYRING, JOHN C.POLANYI und S.SATO haben eine Potentialhyperfläche vorgeschlagen, die nach ihren Entwicklern LEPS genannt wird.
Mathematisch sieht das Potential folgendermaßen aus:
Wobei gilt:
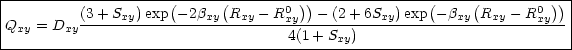
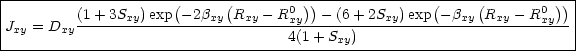
| Es handelt sich um eine Reaktion mit vorgelagertem Gleichgewicht |
Wichtig ist die Massenbilanz:
k1, k2 besitzen die Einheit 1![]() und Kp ist eine einheitslose
Gleichgewichtskonstante.
und Kp ist eine einheitslose
Gleichgewichtskonstante.
Mit der idealen Gasgleichung pV = nRT erhält man:
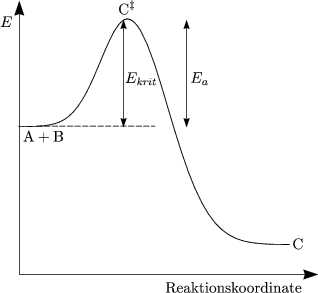
Kp läßt sich prinzipiell bei Kenntnis der Struktur des Übergangszustandes thermodynamisch berechnen (Statistische Thermodynamik).
| Die Geschwindigkeit, mit der AB durch Übergangszustand läuft, hängt zusammen mit Frequenz der charakteristischen Schwingung. |
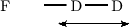
Wir stellen uns vor, daß k† der Schwingungsfrequenz ![]() im Stoßkomplex
entspricht.
im Stoßkomplex
entspricht.
Notwendig für die Berechnung ist:

q ist die molekulare Zustandssumme für jeweilige Spezies, h das Plank’sche
Wirkungsquantum und kB![]()
![]() die BOLTZMANN-Konstante.
die BOLTZMANN-Konstante.