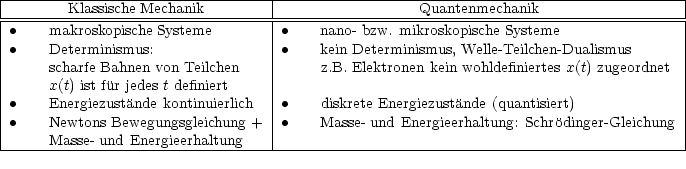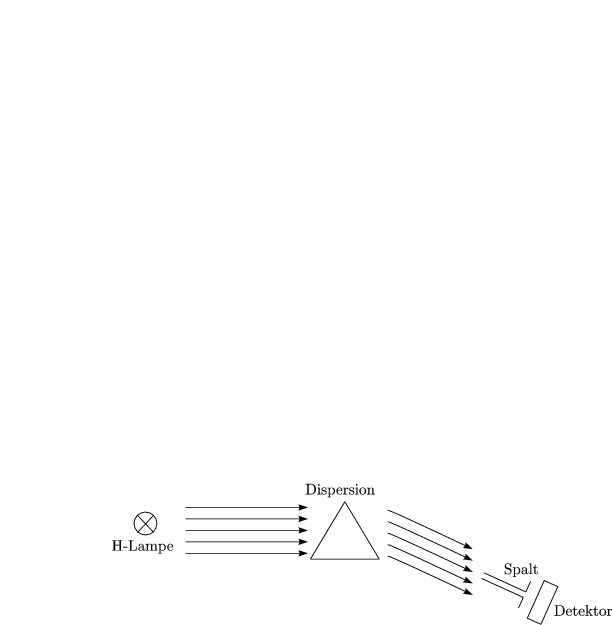

Wir betrachten die elektrische Strahlung von H2 (Emission).
RH ist die Rydberg-Konstante: 109737![]() (109678
(109678![]() ).
).
Somit ist die Energie quantisiert, das heißt diskret.
Die allgemeine Gleichung für Spektrallinien (empirisch gefunden) lautet:
Die Frequenz irgendeiner Spektrallinie ergibt sich aus der Differenz zweier Terme:
Diese Formel ist anwendbar sowohl auf Atome als auch Moleküle.